贵州肝脏中饥饿抑制mTORC1的新机制
近日,基础医学院刘浥课题组研究发现分子生物钟对mTORC1信号通路的调控机制。该研究不仅发现了Per2在调节mTORC1信号通路中的全新功能,还阐明了肝脏中饥饿抑制mTORC1的新机制。
雷帕霉素机能靶标蛋白(mTOR)是一个进化上高度保守的丝氨酸/苏氨酸蛋白激酶,它是为响应环境中营养素与生长因子等信号变化而进行细胞生长与代谢活动的关键调节者。
mTOR存在于两种复合物中,mTOR复合物1(mTORC1)与mTOR复合物2(mTORC2)。这两种复合物受到不同上游信号的调节,产生不同的下游产物。比如,mTORC1信号通路整合至少五种主要的细胞内与细胞外信号——生长因子,压力,能量状态,供氧与氨基酸——来控制蛋白质与脂质合成以及细胞自噬等过程。尽管已有部分研究显示mTORC1信号通路呈现昼夜振荡的规律,并暗示分子生物钟在其中的重要作用,但是分子生物钟调控mTORC1信号通路的具体机制仍未明确。
研究发现,核心节律蛋白Per2能够特异性地与mTORC1发生结合,并作为支架蛋白招募Tsc1到mTORC1,从而特异性地抑制mTORC1的活性。而且,Per2对mTORC1的抑制作用以及mTORC1的振荡规律均取决于Tsc1与mTOR二者的互作强度,且不依赖经典的Tsc1/Tsc2-Rheb通路来实现。
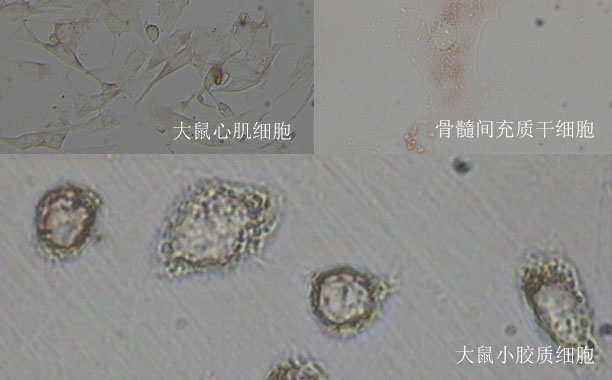
进一步,通过嘌呤霉素摄取实验,细胞增殖实验(MTT),免疫荧光以及透射电镜等技术手段,研究人员发现,Per2缺失能够显著增强蛋白合成与细胞增殖,并强烈抑制体内与体外的自噬过程。此外,在饥饿条件下胰高血糖素-Creb/Crtc2信号流能够诱导Per2的表达,从而发挥对mTORC1信号通路的抑制作用。而由于Per2与Crtc2的缺失所导致的mTORC1的激活效应可通过过表达Per2补偿性逆转。
综上所述,该研究论证了分子生物钟负反馈调节环中的关键蛋白Per2是连接胰高血糖素-Creb/Crtc2信号流与mTORC1信号通路的关键节点。先前已有研究表明Per2是一个抑癌基因,结合mTOR信号通路在癌症中的作用,该研究不仅提出了Per2发挥抑癌作用的新机制,也为治疗癌症以及其他由于mTOR信号紊乱而发生的疾病提供新思路。
雷帕霉素机能靶标蛋白(mTOR)是一个进化上高度保守的丝氨酸/苏氨酸蛋白激酶,它是为响应环境中营养素与生长因子等信号变化而进行细胞生长与代谢活动的关键调节者。
mTOR存在于两种复合物中,mTOR复合物1(mTORC1)与mTOR复合物2(mTORC2)。这两种复合物受到不同上游信号的调节,产生不同的下游产物。比如,mTORC1信号通路整合至少五种主要的细胞内与细胞外信号——生长因子,压力,能量状态,供氧与氨基酸——来控制蛋白质与脂质合成以及细胞自噬等过程。尽管已有部分研究显示mTORC1信号通路呈现昼夜振荡的规律,并暗示分子生物钟在其中的重要作用,但是分子生物钟调控mTORC1信号通路的具体机制仍未明确。
研究发现,核心节律蛋白Per2能够特异性地与mTORC1发生结合,并作为支架蛋白招募Tsc1到mTORC1,从而特异性地抑制mTORC1的活性。而且,Per2对mTORC1的抑制作用以及mTORC1的振荡规律均取决于Tsc1与mTOR二者的互作强度,且不依赖经典的Tsc1/Tsc2-Rheb通路来实现。
进一步,通过嘌呤霉素摄取实验,细胞增殖实验(MTT),免疫荧光以及透射电镜等技术手段,研究人员发现,Per2缺失能够显著增强蛋白合成与细胞增殖,并强烈抑制体内与体外的自噬过程。此外,在饥饿条件下胰高血糖素-Creb/Crtc2信号流能够诱导Per2的表达,从而发挥对mTORC1信号通路的抑制作用。而由于Per2与Crtc2的缺失所导致的mTORC1的激活效应可通过过表达Per2补偿性逆转。
综上所述,该研究论证了分子生物钟负反馈调节环中的关键蛋白Per2是连接胰高血糖素-Creb/Crtc2信号流与mTORC1信号通路的关键节点。先前已有研究表明Per2是一个抑癌基因,结合mTOR信号通路在癌症中的作用,该研究不仅提出了Per2发挥抑癌作用的新机制,也为治疗癌症以及其他由于mTOR信号紊乱而发生的疾病提供新思路。
![贵州吉创生物技术有限公司[官网]](/Public/Uploads/image/picture/160userid20180911_p1536645747.png)