【贵阳生物实验室】:基因编辑技术成功剔除小鼠艾滋病病毒
美国《分子治疗》杂志近日登载了美国天普大学华人科学家胡文辉等人的最新研讨成果:他们应用基因编辑技术,从多靶点高效剔除了一种人源化小鼠多个器官组织中的人类艾滋病病毒,推进基因疗法治疗艾滋病向人体临床实验迈出重要一步。在之前的研讨中,胡文辉团队已胜利应用基因编辑技术,有效肃清了体外培育的人类细胞系、艾滋病患者体内取出的T免疫细胞以及转基因小鼠体内的艾滋病病毒。
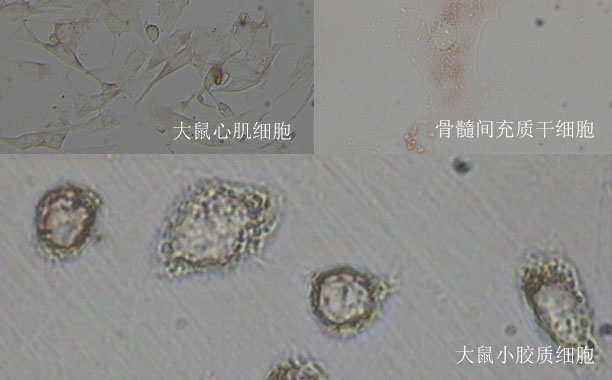
 新研讨更进了一步。他们首先向小鼠体内移植人体骨髓(B)、肝脏(L)和胸腺(T)组织或细胞,"重编程"出人源化BLT小鼠,使其具有与人类一样的艾滋病病毒感染及其埋伏方式。然后,以腺相关病毒(AAV)作为载体,把有"基因魔剪"之称的CRISPR/Cas9基因编辑工具运送到埋伏感染艾滋病病毒的人源化BLT小鼠体内。2到4周后,他们对小鼠多个器官组织停止检测后发现,艾滋病病毒基因组被有效切除。
新研讨更进了一步。他们首先向小鼠体内移植人体骨髓(B)、肝脏(L)和胸腺(T)组织或细胞,"重编程"出人源化BLT小鼠,使其具有与人类一样的艾滋病病毒感染及其埋伏方式。然后,以腺相关病毒(AAV)作为载体,把有"基因魔剪"之称的CRISPR/Cas9基因编辑工具运送到埋伏感染艾滋病病毒的人源化BLT小鼠体内。2到4周后,他们对小鼠多个器官组织停止检测后发现,艾滋病病毒基因组被有效切除。
众所周知,艾滋病病毒基因具有"善变性",胡文辉团队这次提出了一种新思绪,用多靶点基因编辑取代单靶点,以遏制病毒逃逸。他们针对艾滋病病毒转录区和构造区设计了4个导游RNA(核糖核酸),引导Cas9酶到预定位置完成多靶点切除,显着增加了艾滋病病毒的剔除效率。运用"基因魔剪"剔除艾滋病病毒还有一大优点:不影响靶细胞的存活和功用,即"只杀病毒不杀细胞"。
胡文辉表示,目前,基因编辑疗法尚不能100%肃清动物体内的艾滋病病毒,但可以显着降低埋伏的病毒数量,因而它与抗逆转录病毒药物组合,将不失为一种有希望的艾滋病治疗战略。

众所周知,艾滋病病毒基因具有"善变性",胡文辉团队这次提出了一种新思绪,用多靶点基因编辑取代单靶点,以遏制病毒逃逸。他们针对艾滋病病毒转录区和构造区设计了4个导游RNA(核糖核酸),引导Cas9酶到预定位置完成多靶点切除,显着增加了艾滋病病毒的剔除效率。运用"基因魔剪"剔除艾滋病病毒还有一大优点:不影响靶细胞的存活和功用,即"只杀病毒不杀细胞"。
胡文辉表示,目前,基因编辑疗法尚不能100%肃清动物体内的艾滋病病毒,但可以显着降低埋伏的病毒数量,因而它与抗逆转录病毒药物组合,将不失为一种有希望的艾滋病治疗战略。
相关标签:
小鼠艾滋病病毒
本文链接: http://jcswbio.com/news/10232.html
本文链接: http://jcswbio.com/news/10232.html
![贵州吉创生物技术有限公司[官网]](/Public/Uploads/image/picture/160userid20180911_p1536645747.png)